|
|
|
Blog
de Farmacia Roser Miró:
|
|
|
|
FARMACIA.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
PARAFARMACIA
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NOTICIAS
I OFERTAS
|
|
|
 |
Noticias
- Novedades |
|
|
|
|
|
|
TERAPIAS
NATURALES
|
|
|
|
|
|
|
|
MARCAS
Dermocosmética:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

Tf.
00 (376) 867.344

farmaciamiro@andorra.ad
|
|
Blog
de Farmacia Roser Miró. Andorra.
|
|
REALIZAR
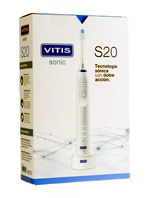
UNA CORRECTA HIGIENE BUCAL
|
REALIZAR
UNA CORRECTA HIGIENE BUCAL
Artículo
elaborado el 14/02/2020, por Farmacia Roser Miró Tuset.
La alimentación
diaria hace que queden restos de comida entre los dientes o
adheridos a ellos. Estos se acumulan y forman la llamada placa
bacteriana.
Reducir
la placa bacteriana disminuye el riesgo de caries, de gingivitis
o inflamación de las encías, de periodontitis
y de halitosis, que a largo plazo pueden derivar en problemas
bucales más graves […]
CONTINUAR
LEYENDO ?
|
|
CORONAVIRUS
DE WUHAN

|
CORONAVIRUS
DE WUHAN
Artículo
elaborado el 27/01/2020, por Farmacia Roser Miró Tuset.
El coronavirus
de Wuhan, también conocido como nuevo coronavirus (2019-nCoV),
es un virus que pertenece a la familia de los coronavirus ARN
monocatenario positivo. Los científicos creen que las
enfermedades podrían haberse originado de la Bungarus
multicinctus, una serpiente altamente venenosa en el Mercado
de Alimentos de Wuhan (China).
Los coronavirus son una gran familia de virus que pueden causar
enfermedades respiratorias en el hombre y en los animales, desde
un resfriado común hasta una neumonía potencialmente
mortal o enfermedades más graves, como el Síndrome
Respiratorio del Medio Oriente (MERS) y el Síndrome Respiratorio
Agudo Severo (SARS).
Los síntomas habituales son fiebre y síntomas
respiratorios (tos y disnea o dificultad para respirar). En
los casos más graves, estas infecciones pueden causar
neumonía, síndrome respiratorio agudo severo,
insuficiencia renal e, incluso, la muerte.
[…]
CONTINUAR
LEYENDO ?
|
|
OSTEOPOROSIS
EN PERSONAS JOVENES

|
OSTEOPOROSIS
EN PERSONAS JOVENES
PUBLICADO
el 17/01/2020, a partir de un artículo de la farmacéutica
titular Roser Miró Tuset, en la revista Dona Secret Núm.
51.
La osteoporosis
es una enfermedad silenciosa, que no produce dolor, y solemos
descubrirla cuando aparece una fractura especialmente en las
caderas, las muñecas o la columna. El hueso se debilita
porque la generación de células óseas nuevas
es más lenta que su deterioro. Aparece en personas de
edad avanzada y suele estar relacionada con los cambios hormonales:
en las mujeres aumenta cuando disminuyen los estrógenos;
en los hombres, cuando disminuye la testosterona; al aumentar
la presencia de hormonas tiroidales y con la hiperactividad
paratiroidal y suprarrenal.
[…]
CONTINUAR
LEYENDO ?
|
|
PIOJOS Y
LIENDRES.
Que
son? Como prevenirlos? Que tratamiento usar en caso de contagio?

|
PIOJOS
PUBLICADO
el 30/07/2019 por Equipo farmacéuticos de Farmacia Roser
Miró
Los piojos
son pequeños insectos, de unos 2mm., que viven en la
cabeza de las personas. Son parásitos y necesitan alimentarse
de sangre humana para sobrevivir. Sus huevos, llamados liendres,
son aún más pequeños, parecidos a la escama
de caspa. Los piojos no pueden saltar, ni volar, por tanto,
para contagiarse, es […]
CONTINUAR
LEYENDO ?
|
|
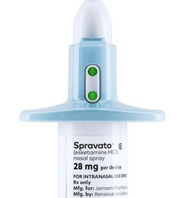
Spravato
(Sketamina HCI) de laboratorios Janssen.
|
Spravato
(Sketamina HCI) de laboratorios Janssen.
EEUU ha
aprobado en fecha 5 de marzo del 2019 la comercialización
de Spravato (Sketamina HCI) de laboratorios Janssen, un nuevo
antidepresivo en forma de espray nasal.
El Spravato
promete una rápida eficacia pero debe consumirse en un
consultorio o en una clínica bajo supervisión
médica, debido al potencial abuso que puede provocar.
La máxima
autoridad sanitaria de Estados Unidos (FDA) ha aprobado el que
se califica como un revolucionario tratamiento para la depresión.
El compuesto del medicamento es la esketamina y se comercializará
en forma de espray nasal bajo el nombre de Spravato, distribuido
por Janssen. El nuevo fármaco está pensado para
las personas que ya hayan probado otros medicamentos de este
tipo.
La FDA restringió
la distribución del fármaco, ordenando su uso
bajo vigilancia médica, debido al "potencial de
abuso" que puede provocar. El tratamiento recomendado es
consumirlo dos veces a semana, durante un mes, con refuerzos
si es necesario, mientras se toma un antidepresivo oral de uso
común.
|
|
BONECO
P50.

Precio
BONECO P50: 55,65€
|
BONECO
P50.
Ionizador, purificador y difusor de aromas.
Boneco P50
es un purificador, ionizador y difusor de aromas 2 en 1, que
funciona sin agua diseñado para viajar o para uso personal.
Es compacto
y se enchufa con USB C, de manera que se puede transportar fácilmente
a cualquier lugar donde vaya.
Incluye
un cartucho de aroma de larga duración para dispersar
el olor de aceites esenciales o perfumes.
El ionizador
genera iones negativos que ayudan a reducir las partículas
al aire y lo puedes enchufar o desenchufar según tus
necesidades.
El P50 es
un producto perfecto para crear un ambiente saludable a tu alrededor.
|
|
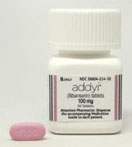
Addyi
(La Viagra femenina).
|
La Administración
de alimentos y Medicamentos de Estados Unidos (FDA) ha aprobado
la comercialización de "Addyi", conocida como
la Viagra Femenina. Por su color se la conoce también
como la píldora rosa, y se trata del primer tratamiento
autorizado para incrementar el deseo sexual.
Su principio
activo es la flibanserina, y tiene como propósito liberar
una serie de neurotransmisores en el cerebro para incentivar
el deseo. Estimula dos componentes químicos considerados
factores de excitación sexual en el cerebro, la dopamina
y la norepinefrina y reduce un tercero, la serotonina que hace
descender la libido.
"Addyi"
no funciona como en el caso de la Viagra masculina el día
que se va a tener relaciones sexuales para que estas sean más
placenteras, sino que está pensada como un tratamiento
continuo que consiste en tomar una pastilla diaria.
Fuente y
más información: http://www.fda.gov/NewsEvents/Newsroom/ComunicadosdePrensa/ucm458939.htm
|
|
Kalia™
de Intimina.

Precio:
82,97€
|
Debido a
que más del 80% de las mujeres relatan no conseguir el
orgasmo con sus parejas, éstas empiezan a buscar nuevas
prácticas para animar su intimidad. Sus beneficios son
más que los evidentes. Los masajeadores para parejas
Kalia™ permiten nuevas formas de reavivar los juegos íntimos
y activan la intensidad del placer para tener una relación
más feliz y saludable.
Kalia™
de Intimina,
es un masajeador para parejas sutilmente diseñado para
ser llevado por la mujer durante las relaciones íntimas.
Recubierto con silicona suave y flexible, sus silenciosas vibraciones
brindan placeres internos y externos simultáneamente
a ambos miembros de la pareja. KaliaTM es el accesorio perfecto
para descubrir juntos nuevas experiencias íntimas y alcanzar
una nueva dimensión de placer.
Beneficios:
• Fabricado con silicona y plástico ABS aprobados
por la FDA; ambos sin látex ni ftalatos, no porosos para
evitar la acumulación de suciedad y bacterias
• Completamente sumergible para facilitar su limpieza y
disfrute bajo el agua
• Interfaz de un único botón que ofrece un
control intuitivo de sus 6 modos de vibración
• Recargable por USB para mayor comodidad.
|
|
Celesse
de Intimina.

Precio:
44,20€
|
Celesse
de Intimina,
es un masajeador personal con un diseño curvado creado
específicamente para la estimulación interna.
Es resistente al agua y está recubierto de la más
suave silicona, apta para el contacto con la piel. Sus controles
son sencillos de utilizar y las vibraciones son muy silenciosas.
Celesse cuenta con 6 modos rítmicos y 16 velocidades
para ofrecer una gran variedad de experiencias positivas.
En Intimina
sabemos que cada mujer es única y reconocemos la individualidad
de cada una de ellas. Kiri, Raya y Celesse han sido diseñados
con esta premisa en mente, adaptándose a las diferentes
formas en que cada mujer disfruta de su intimidad.
Además
de las razones obvias, disfrutar con frecuencia de cierta actividad
íntima es beneficioso para tu salud general y tu bienestar
físico y mental. La estimulación sensual alivia
el estrés y mejora la circulación.
|
|
La agencia
estadounidense del medicamento (FDA) ha autorizado un nuevo
fármaco para ayudar a pacientes obesos a perder peso.
Qsymia se convierte así en el segundo tratamiento
autorizado con este fin en pocas semanas, después de
que las autoridades de EEUU diesen luz verde a Belviq, el primer
tratamiento para el sobrepeso y la obesidad aprobado desde 1999.
COMUNICADO
DE PRENSA DE LA FDA. Fuente: FDA (Administración de Alimentos
y Medicamentos de los Estados Unidos). www.fda.gov
"Para
su publicación inmediata: 17 de julio de 2012
Aprueba
la FDA el medicamento Qsymia para bajar de peso
La Administración de Alimentos y Medicamentos de los
Estados Unidos (FDA en inglés) aprobó Qsymia (fentermina
y topiramato de liberación prolongada) como complemento
a una dieta con menos calorías y ejercicio para el control
del sobrepeso crónico.
El medicamento está aprobado para adultos con un índice
de masa corporal (IMC) de 30 o más (obesos) o adultos
con un IMC de 27 o más (sobrepeso) y que tengan por lo
menos un padecimiento relacionado con el peso, tales como presión
arterial alta (hipertensión), diabetes tipo 2 o colesterol
alto (dislipidemia).
El IMC, que mide la grasa en el cuerpo según el peso
y la altura de la persona, se usa para definir las categorías
de obesidad y sobrepeso. Según los Centros para el Control
y la Prevención de Enfermedades, más de una tercera
parte de los adultos en los Estados Unidos sufre de obesidad.
«La obesidad amenaza el bienestar general de los pacientes
y es una preocupación de salud pública importante»,
expresó la Dra. Janet Woodcock, directora del Centro
para la Evaluación e Investigación de Medicamentos
de la FDA. «Qsymia, si se usa responsablemente combinada
con un estilo de vida saludable que incluya una dieta con menos
calorías y ejercicio, brinda otra opción de tratamiento
para el control de peso crónico para las personas en
los EE.UU. que son obesas o sufren de sobrepeso y que tengan
por lo menos una afección comórbida relacionada
con el peso.»
Qsymia es una combinación de dos medicamentos aprobados
por la FDA, la fentermina y el topiramato, en una fórmula
de liberación prolongada. La fentermina sirve para la
pérdida de peso a corto plazo en adultos con sobrepeso
o adultos obesos que hagan ejercicios y lleven una dieta con
menos calorías. El topiramato sirve para tratar ciertos
tipos de convulsiones en las personas que tienen epilepsia y
evitar migrañas.
Qsymia no se debe usar durante el embarazo porque puede dañar
al feto. Los datos demuestran que un feto expuesto al topiramato,
un componente de Qsymia, durante el primer trimestre del embarazo
tiene un riesgo mayor de nacer con malformaciones orales (labio
leporino con o sin paladar hendido). Las mujeres en edad reproductiva
no deben estar embarazadas cuando comiencen la terapia con Qsymia
ni quedar embarazadas mientras tomen Qsymia. Las mujeres en
edad reproductiva deben hacerse una prueba de embarazo que resulte
negativa antes de comenzar a tomar Qsymia, y luego una prueba
mensual mientras tomen el medicamento. Además deben usar
métodos anticonceptivos eficaces de manera consistente
mientras tomen Qsymia.
La seguridad y eficacia de Qsymia fueron evaluadas en dos estudios
clínicos aleatorios, controlados por placebo, que incluyeron
aproximadamente a 3,700 pacientes obesos y con sobrepeso, con
y sin padecimientos significativos relacionados al sobrepeso,
y fueron tratados durante un año. A todos los pacientes
se les modificó su estilo de vida con una dieta con menos
calorías y actividad física regular.
La dosis diaria recomendada para Qsymia es de 7.5 miligramos
de fentermina y 46 mg de topiramato de liberación prolongada.
Qsymia también está disponible en una dosis más
alta (15 mg de fentermina y 92 mg de topiramato de liberación
prolongada) para ciertos pacientes.
Los resultados de los dos estudios clínicos demostraron
que después de un año de tratamiento con la dosis
recomendada y la dosis más alta de Qsymia, los pacientes
tuvieron una pérdida de peso de 6.7 por ciento y 8.9
por ciento respectivamente más en comparación
con los que tuvieron tratamiento con el placebo. Aproximadamente
el 62 por ciento y el 69 por ciento de los pacientes perdieron
por lo menos un cinco por ciento de su peso corporal con la
dosis recomendada y la dosis mayor de Qsymia, respectivamente,
comparado con aproximadamente el 20 por ciento de los pacientes
tratados con placebo.
Los pacientes que no perdieron al menos el tres por ciento de
su peso corporal para la semana 12 del tratamiento con Qsymia
tuvieron pocas probabilidades de lograr y mantener una pérdida
de peso sostenida al continuar el tratamiento con esta dosis.
Por lo tanto, es necesario evaluar la respuesta a la terapia
con la dosis recomendada de Qsymia por 12 semanas para determinar,
según la cantidad de pérdida de peso, si se debe
descontinuar el tratamiento con Qsyimia o aumentarlo a la dosis
más alta. Si después de 12 semanas tomando la
dosis más alta de Qsymia, el paciente no pierde por lo
menos cinco por ciento de su peso corporal, entonces debe descontinuar
el uso de Qsymia, puesto que es poco probable que estos pacientes
logren una pérdida de peso clínicamente significativa
al continuar el tratamiento.
Los pacientes con glaucoma o hipotiroidismo no deben usar Qsymia.
Qsymia puede aumentar el ritmo cardíaco y se desconocen
los efectos de esta droga en el ritmo cardíaco de pacientes
con alto riesgo de ataque cardíaco o infarto. Por lo
tanto, no está recomendado el uso de Qsymia para pacientes
con enfermedades cardíacas recientes (en los últimos
seis meses) o con una enfermedad cardíaca inestable o
que hayan tenido un infarto. Se recomienda vigilar regularmente
el ritmo cardíaco de todos los pacientes que toman Qsymia,
especialmente al comenzar a tomar Qsymia o aumentar la dosis.
La FDA aprobó Qsymia con una Estrategia de Evaluación
y Mitigación de Riesgos (REMS, por sus sigla en inglé)
que consiste en una Guía de Medicación para orientar
a los pacientes sobre la información y elementos de seguridad
importantes para asegurar el uso seguro que incluye la capacitación
de los que prescriben el medicamento y la certificación
de las farmacias. El propósito de la REMS es educar a
los que recetan el medicamento y a sus pacientes sobre el alto
riesgo de defectos congénitos asociados con la exposición
a Qsymia durante el primer trimestre del embarazo, la necesidad
de la prevención del embarazo y la necesidad de descontinuar
la terapia si hay un embarazo. Qsymia sólo estará
disponible en farmacias especialmente certificadas.
Vivus Inc. tendrá la obligación de llevar a cabo
10 requisitos de postcomercialización, incluyendo un
estudio clínico de resultados cardiovasculares a largo
plazo para evaluar el efecto de Qsymia sobre el riesgo de eventos
cardíacos significativos adversos, tales como ataques
cardiacos e infartos.
Los efectos secundarios más comunes de Qsymia son hormigueo
en las manos y los pies (parestesia), mareo, sensación
de alteración del gusto, insomnio, estreñimiento
y boca seca.
Qsymia está comercializado por Vivus Inc. en Mountain
View, California."
|
|
FDA aprueba
BELVIQ, el primer tratamiento para la obesidad que aprueba
en 13 años, desde 1999.
COMUNICADO
DE PRENSA DE LA FDA. Fuente: FDA. www.fda.gov
La FDA aprueba
Belviq para tratar a algunos adultos con sobrepeso u obesos
La Administración de Alimentos y Medicamentos de los
Estados Unidos aprobó hoy Belviq (clorhidrato de lorcaserina),
como complemento de una dieta reducida en calorías y
ejercicio y para el tratamiento del sobrepeso crónico.
El fármaco
se aprobó para uso en adultos con un índice de
masa corporal (IMC) de 30 o superior (obesos), o con un IMC
de 27 o superior (sobrepeso) y que tienen al menos una enfermedad
relacionada con el peso, como alta presión arterial (hipertensión),
diabetes tipo 2 o alto nivel de colesterol (dislipidemia).
El IMC,
que mide las grasas corporales en base al peso y la altura de
la persona, se utiliza para definir las categorías de
obesidad y sobrepeso. De acuerdo con los Centros para el Control
y la Prevención de Enfermedades, más de un tercio
de los adultos en los Estados Unidos son obesos.
“La obesidad amenaza el bienestar general de los pacientes
y es uno de los problemas principales de la salud pública”,
dijo la Dra. Janet Woodcock, directora del Centro de Evaluación
e Investigación de Medicamentos de la FDA. “La aprobación
de este fármaco, utilizado de manera responsable en combinación
con una dieta y un estilo de vida saludables, ofrece una opción
de tratamiento para los estadounidenses que son obesos o tienen
sobrepeso y tienen al menos una enfermedad comórbida
relacionada con el peso”.
Belviq funciona activando el receptor de serotonina 2C en el
cerebro. La activación de este receptor puede ayudar
a la persona a comer menos y sentirse satisfecha luego de comer
pequeñas cantidades de alimentos.
La seguridad y la eficacia de Belviq se evaluaron en tres estudios
aleatorizados, controlados con placebo que incluyeron a casi
8,000 pacientes obesos y con sobrepeso, con y sin diabetes tipo
2, tratados durante 52 y hasta 104 semanas. Todos los participantes
recibieron asesoramiento sobre la modificación del estilo
de vida que incluyó una dieta reducida en calorías
y ejercicios. En comparación con el placebo, el tratamiento
con Belviq durante un año estuvo asociado con una reducción
promedio del peso del 3 por ciento al 3.7 por ciento.
Aproximadamente el 47 por ciento de los pacientes sin diabetes
tipo 2 bajó como mínimo un 5 por ciento de su
peso corporal en comparación con aproximadamente el 23
por ciento de los pacientes tratados con placebo. En las personas
con diabetes tipo 2, aproximadamente el 38 por ciento de los
pacientes tratados con Belviq y el 16 por ciento de los tratados
con placebo bajó como mínimo un 5 por ciento de
peso corporal. El tratamiento con Belviq estuvo asociado con
cambios favorables en el control glucémico en las personas
que tenían diabetes tipo 2. Las indicaciones aprobadas
para Belviq recomiendan interrumpir la administración
del fármaco en los pacientes que no bajen el 5 por ciento
de peso corporal al cabo de 12 semanas de tratamiento, ya que
es poco probable que estos pacientes logren una reducción
del peso clínicamente significativa con un tratamiento
continuado.
Belviq no debe utilizarse durante el embarazo. El tratamiento
con Belviq puede causar efectos colaterales graves, incluyendo
síndrome serotoninérgico, en particular cuando
se toma con determinados medicamentos que aumentan los niveles
de serotonina o activan los receptores de serotonina. Se incluyen,
entre otros, los fármacos habitualmente utilizados para
tratar la depresión y la migraña. Belviq también
puede causar trastornos en la atención o la memoria.
En 1997, los fármacos para reducir el peso fenfluramina
y dexfenfluramina fueron retirados del mercado después
de que surgieran evidencias de que causaban daño en las
válvulas cardíacas. Se supone que este efecto
está relacionado con la activación del receptor
de serotonina 2B del tejido cardíaco. Cuando se utiliza
a la dosis aprobada de 10 miligramos dos veces al día,
Belviq no parece activar al receptor de serotonina 2B.
La función de la válvula cardíaca se evaluó
mediante ecocardiografía en casi 8000 pacientes del programa
de desarrollo de Belviq. No hubo una diferencia estadísticamente
significativa en el desarrollo de anomalías valvulares
según la definición de la FDA entre los pacientes
tratados con Belviq y placebo. Dado que los datos preliminares
sugieren que la cantidad de receptores de serotonina 2B puede
verse aumentada en los pacientes con insuficiencia cardíaca
congestiva, Belviq debe utilizarse con precaución en
los pacientes que tengan esta enfermedad. No se ha estudiado
Belviq en pacientes con valvulopatías cardíacas
graves.
El fabricante del fármaco deberá realizar seis
estudios post-comercialización, incluyendo un estudio
de los resultados cardiovasculares a largo plazo para determinar
el efecto de Belviq sobre el riesgo de eventos cardíacos
adversos importantes como ataque cardíaco y accidente
cerebrovascular.
Los efectos colaterales más comunes de Belviq en los
pacientes no diabéticos son dolor de cabeza, mareos,
fatiga, náuseas, sequedad bucal y estreñimiento,
y en los pacientes diabéticos son bajo nivel de azúcar
en sangre (hipoglucemia), dolor de cabeza, dolor de espalda,
tos y fatiga.
Belviq es fabricado por Arena Pharmaceuticals GmbH de Zofingen,
Suiza, y distribuido por Eisai Inc. de Woodcliff Lake, N.J.
|
| 29
de febrero de 2012.- Se prohíbe cautelarmente la
comercialización de los genéricos de sildenafilo
(Viagra).
Pfizer es
la titular de la patente de sildenafilo, un principio activo
que comercializa para el tratamiento de la disfunción
eréctil y la hipertensión arterial pulmonar.
|
|
Nuevo
envase Viagra:
Pfizer ha
notificado que modificará en breve el embalaje de su
medicamento 'Viagra' con el objetivo de que se identifiquen
mejor los auténticos comprimidos frente a las falsificaciones.
Los cambios se han realizado tanto en el embalaje exterior como
en el blíster de aluminio interior.
El nuevo
envase exterior incluye un dispositivo de última generación
y nuevas medidas de seguridad, tanto visibles -como el uso de
tinta ópticamente variable- como invisibles. Asimismo,
se unificará el modelo del blíster interior en
todas las presentaciones.
|
| La
FDA (Administración Federal de Fármacos del Gobierno
de EEUU), ha aprobado el uso de BÓTOX en terapias contra
migrañas severas y crónicas.
La FDA indicó
el tratamiento, exclusivamente para migrañas crónicas,
y que recomienda el uso de bótox aproximadamente cada
12 semanas, mediante inyecciones múltiples en torno a
la cabeza y el cuello para aliviar los síntomas.
La FDA insistió,
sin embargo, que el bótox, fabricado por la empresa Allergan,
no ha demostrado eficacia para tratar migrañas más
leves, aquellas que ocurren durante 14 días o menos por
mes, o para otros tipos de dolores de cabeza.
La FDA también
recomendó que los pacientes consulten a su médico
sobre el uso de Botox para su caso particular.
Encontrará
más información acerca del Bótox, así
como su prospecto, en nuestra página exclusiva para vistabel:
www.farmaciaandorra.com/vistabel.
|
|
Fertil
Marq

|
Test de
concentración de espermatozoides en el semen:
- Rápido
y sencillo
- Seguro
- Privado
|
|
30
Day Beauty Secret

|
30 Day Beauty
Secret (Futurebiotics)
Nuevo complemento
alimentario revolucionario en el campo de la belleza de la mujer.
Proporciona al cuerpo una exclusiva combinación de todas
las vitaminas y minerales esenciales.
|
|
Tiger
Liniment
|
Aceite
para masaje a base de mentol, alcanfor, eucalipto, ...para calmar
el dolor de músculos y articulaciones. Utilizado para
dolores de espalda, artritis, en contracturas musculares, golpes,
etc.
|
|